История открытия азота и его истолкование, строение атома и молекулы, физические и химические свойства азота, а также его применение в различных областях.
Cодержание
История открытия
В 1772 году Генри Кавендиш провел опыт, в результате которого был выделен азот. Однако, он не смог понять, что это новое простое вещество, и описал его как "удушливый воздух". В том же году Кавендиш сообщил об этом опыте Джозефу Пристли. В то время Пристли также получал азот, но неверно истолковал его как "флогистированный воздух". В сентябре 1772 года Даниэль Резерфорд опубликовал диссертацию, в которой описал азот как вредный, ядовитый воздух и предположил, что это новый химический элемент.
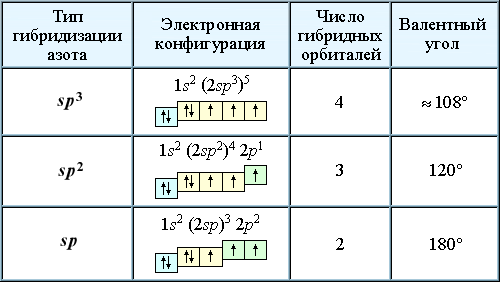
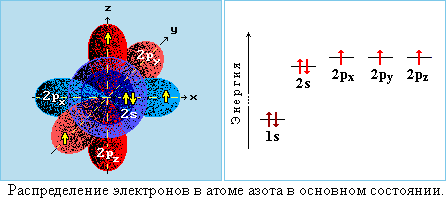
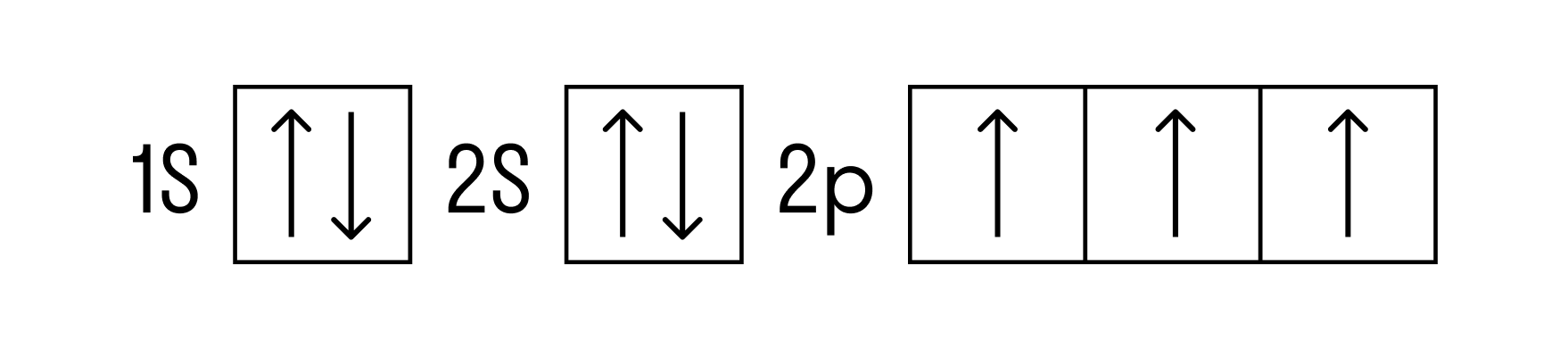
Строение атома и электронная конфигурация азота
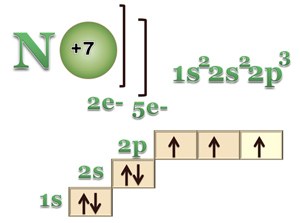
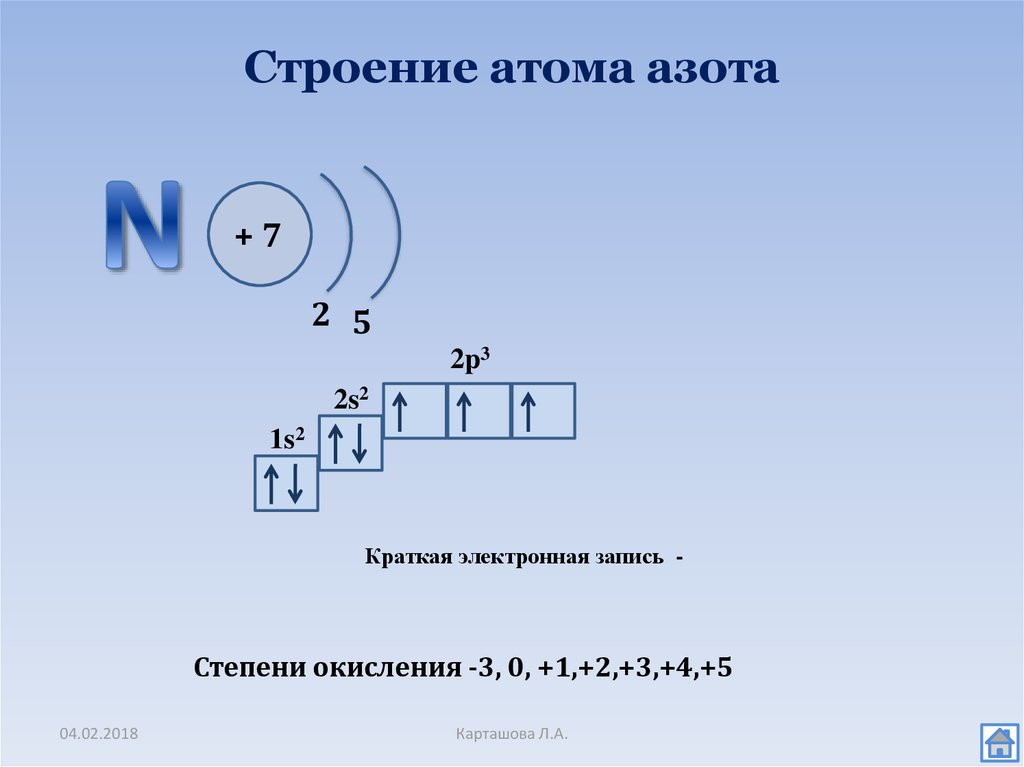
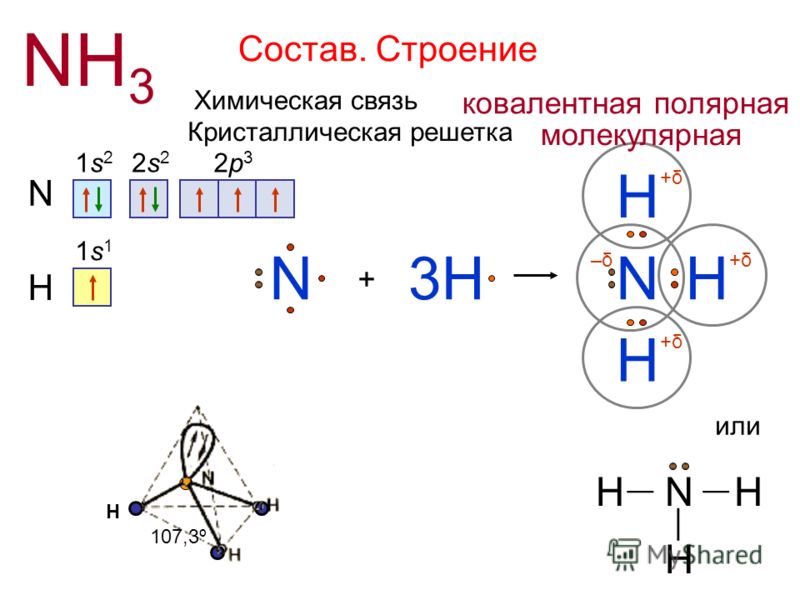
Азот (N) является седьмым элементом периодической таблицы, расположенным в пятой группе и втором периоде. У азота относительная атомная масса равна 14. Атом азота состоит из ядра с зарядом +7 и семи электронов, распределенных по двум энергетическим уровням. В основном состоянии электронная формула азота: 1s2 2s2 2p3, в сокращенном виде - [He]2s2 2p3. На внешнем энергетическом уровне у азота находится 5 валентных электронов, среди которых 3 неспаренных p-электрона.
Строение молекулы азота
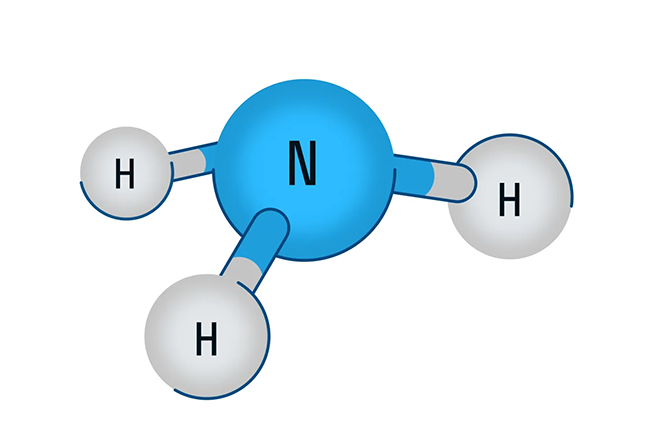
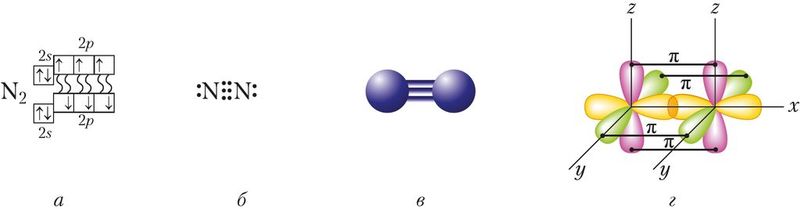
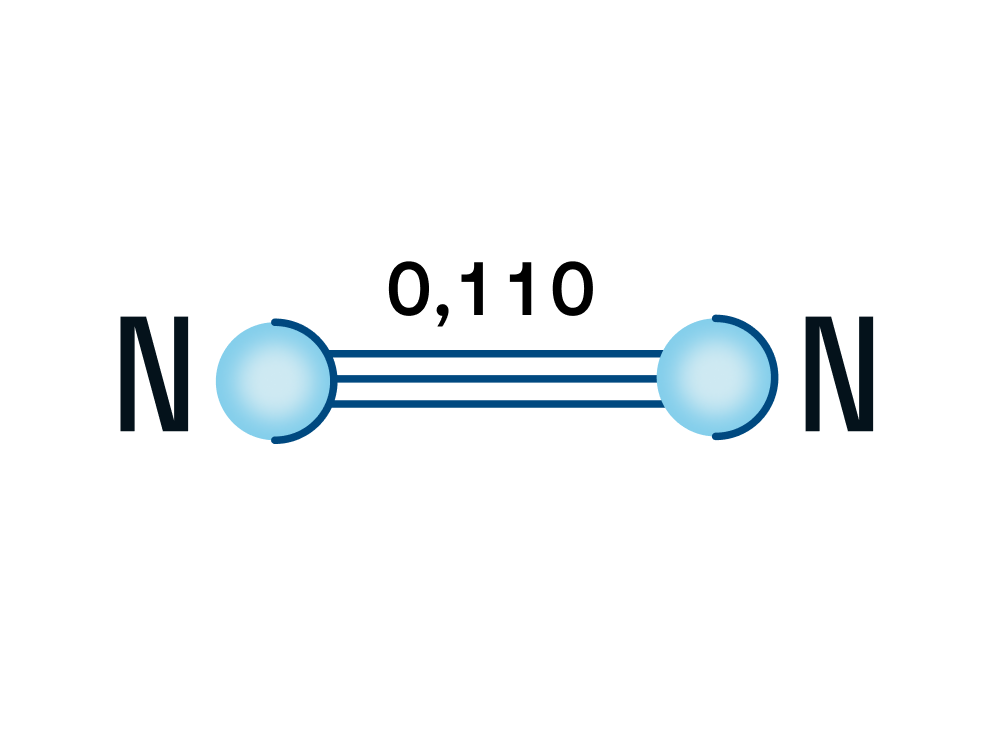
Молекула азота (N2) является двухатомной и атомы связаны между собой прочной тройной связью. Длина связи составляет 0,110 нм. Каждый атом азота имеет 3 неспаренных электрона, которые образуют тройную связь, состоящую из одной сигма-связи и двух пи-связей.
См. также
Физические свойства азота
Азот (N2) является бесцветным газом без запаха и вкуса. Он плохо растворяется в воде и легче, чем воздух, по своей молярной массе. Температура плавления азота составляет -210 °C, а температура кипения -196 °C. Азот не образует аллотропных модификаций.
Химические свойства азота
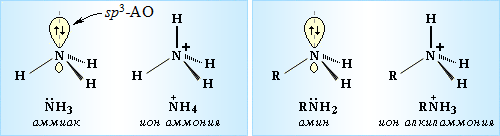
Азот (N) является малоактивным элементом из-за наличия тройной связи между атомами в молекуле азота. Он соединяется с другими элементами при высоких температурах. Атомы азота могут образовывать соединения с металлами и неметаллами, которые называются нитридами. Азот может иметь степень окисления от -3 до +5.
Применение азота
Азот широко применяется в промышленности, особенно жидкий азот используется для охлаждения и замораживания. Он также используется в производстве аэрозолей и как окислитель в двигателях ракет. Азот входит в состав аминокислот и нуклеотидов, и его присутствие необходимо для построения белков и ДНК.