Кислород (химический символ - O) является химическим элементом второго периода периодической системы Д. И. Менделеева с атомным номером 8. Он относится к 16-й группе (по устаревшей классификации - главной подгруппе шестой группы, VIA). Кислород является химически активным неметаллом и самым легким элементом из группы халькогенов. Узнайте все о ионизации кислорода, энергии ионизации и связи с озоном.
Кислород (химический символ - O) является химическим элементом второго периода периодической системы Д. И. Менделеева с атомным номером 8. Он относится к 16-й группе (по устаревшей классификации - главной подгруппе шестой группы, VIA). Кислород является химически активным неметаллом и самым легким элементом из группы халькогенов.
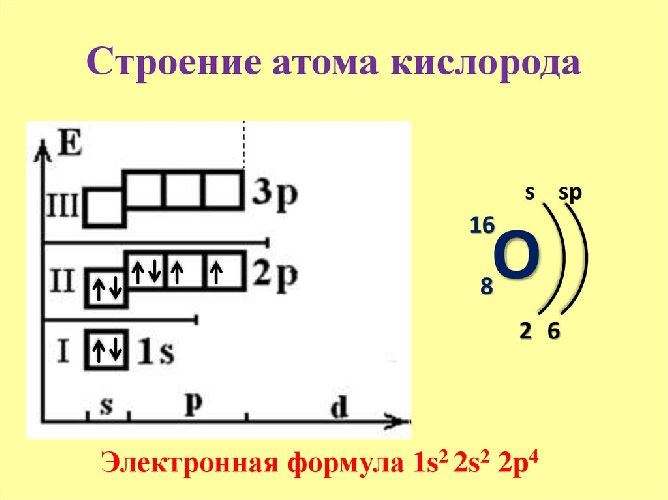
Ионизация - процесс отрыва электрона от атома. Энергия, необходимая для отрыва электрона от атома, называется энергией ионизации. В случае кислорода, учитывая первый электрон, ионизация обозначается как Eo.

Энергия ионизации кислорода
Чем ближе электрон к центру атома, тем больше энергии требуется для его отрыва. Конкретное значение энергии ионизации кислорода зависит от конкретного электрона в рассматриваемой системе. Обычно, при обсуждении энергии ионизации, речь идет о первом электроне, так как он обладает наибольшей энергией ионизации.
Официально считается, что кислород был открыт английским химиком Джозефом Пристли 1 августа 1774 года. Он разложил оксид ртути в герметично закрытом сосуде с помощью солнечных лучей. Однако, Пристли не понял, что открыл новое простое вещество и считал, что выделил одну из составных частей воздуха. Вскоре после этого, французский химик Антуан Лавуазье установил, что кислород является составной частью воздуха, кислот и содержится во многих веществах.

Озон и ионизация кислорода
Кислород может образовывать различные аллотропные формы, включая озон. Озон - это газ голубого цвета со специфическим запахом, молекула которого состоит из трех атомов кислорода (O3). Он образует озоновый слой в стратосфере, который формируется за счет ионизации кислорода ультрафиолетовым излучением.
Ионизация кислорода приводит к образованию дважды ионизированного иона O2+. Он также может существовать в виде газа, состоящего из таких ионов. В спектроскопии он обозначается как [O III].
Яркие эмиссионные линии [O III] наблюдаются в диффузных и планетарных туманностях. Они находятся в зеленой части спектра, с основной линией, имеющей длину волны 500,7 нм, и менее интенсивной линией с длиной волны 495,9 нм. Эти линии были сначала обнаружены в спектрах планетарных туманностей в 1860-х годах и ошибочно приписывались новому элементу, названному небулием. Однако в 1927 году Айра Спрэг Боуэн доказал, что эти линии излучаются атомами дважды ионизированного кислорода.
Ионизация кислорода может также приводить к образованию других ионов и эмиссионных линий, включая те, которые находятся в инфракрасной области спектра.
См. также
Что нам скажет Википедия?
Как простое вещество (при нормальных условиях) кислород — газ без цвета, вкуса и запаха, молекула которого состоит из двух атомов (формула — O2). Систематическое название: дикислород.
Жидкий кислород (при низких температурах) имеет светло-голубой цвет, а твёрдый (при низких температурах) представляет собой кристаллы светло-синего цвета.
Существуют и другие аллотропные формы кислорода, например, озон — при нормальных условиях газ голубого цвета со специфическим запахом, молекула которого состоит из трёх атомов кислорода (формула O3). Систематическое название: трикислород. Часто можно почувствовать запах озона после грозы. Озон образует озоновый слой в стратосфере, который образуется там за счёт ионизации кислорода ультрафиолетом.