Идея о том, что материя состоит из отдельных единиц, очень стара. Узнайте, как возник термин "атом" и его значение в древнегреческой философии. Познакомьтесь с развитием научного понимания атома и современной моделью его строения. Узнайте, какие свойства атома определяют его состав и подчиняются квантовым законам. - NOCFN
Cодержание
Философский атомизм
Идея о том, что материя состоит из отдельных единиц, очень стара. Она появилась во многих древних культурах, таких как Греция и Индия. Слово «атом» др.-греч. ἄτομος, что означает «неразрезаемый», был придуман досократическим греческим философом Левкиппом и его учеником Демокритом (460—370 до н.э.). Демокрит учил, что количество атомов бесконечно, они несоздаваемы и неуничтожимы, и являются основой всего существующего. Атомы каждого элемента индивидуальны по строению и свойствам и обозначаются химическими символами элементов. Атомы могут существовать как в свободном состоянии, так и в связанном.

Развитие научного понимания атома
В начале 1800-х годов учёный Джон Дальтон заметил, что химические вещества, казалось, объединяются и распадаются на другие вещества по массе. Некоторые предполагали, что каждый химический элемент в конечном итоге состоит из крошечных неделимых частиц постоянной массы. Вскоре после 1850 года некоторые физики разработали кинетическую теорию газов и тепла, которая математически описывала поведение газов, предполагая, что они состоят из частиц.
В начале 20 века Альберт Эйнштейн и Жан Перрен доказали, что броуновское движение (беспорядочное движение зёрен пыльцы в воде) вызвано действием молекул воды. Эти эксперименты стали третьей линией доказательств существования атомов и молекул.
На протяжении девятнадцатого века некоторые учёные предостерегали, что доказательства существования атомов являются косвенными, и атомы на самом деле могут не быть реальными, а только казаться таковыми.
К началу 20 века учёные разработали довольно подробные и точные модели структуры материи, что привело к более строгой классификации невидимых частиц, составляющих обычную материю. Атом теперь определяется как основная частица, составляющая химический элемент. Примерно на рубеже 20-го века физики обнаружили, что частицы, которые химики назвали «атомами», на самом деле являются скоплениями ещё более мелких частиц (субатомных частиц). Сейчас термин элементарная частица используется для обозначения фактически неделимых частиц, а атомы остаются самыми мелкими частицами, неделимыми химически.

Современное представление о строении атома
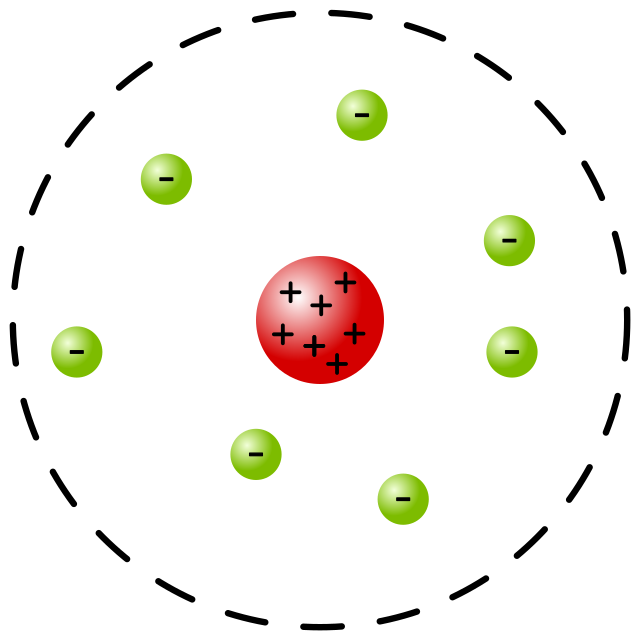
Атом состоит из тяжёлого ядра, обладающего положительным электрическим зарядом, и окружающих его лёгких электронов с отрицательными электрическими зарядами, образующих электронные оболочки атома. Размеры атома определяются размерами его внешней электронной оболочки и велики по сравнению с размерами ядра атома.
Характерные порядки размеров:
| Объект | Диаметр | Площадь поперечного сечения | Объём |
|---|---|---|---|
| Атом | 10^-8 см | 10^-16 см^2 | 10^-24 см^3 |
| Ядро | 10^-12 см | 10^-24 см^2 | 10^-36 см^3 |
Свойства макроскопических тел - газообразных, жидких и твёрдых - и свойства отдельных молекул зависят от свойств входящих в их состав атомов. Все свойства атома определяются его строением и подчиняются квантовым законам.
См. также
Заключение
Таким образом, термин "атом" возник из древнегреческой философии, где он означал "неразрезаемый". С течением времени и развитием научных идей, представление о строении атома менялось. Современная модель атома объясняет его состав и свойства, но оказывается, что сам атом состоит из еще более мелких субатомных частиц. Несмотря на это, термин "атом" остается применяемым для обозначения основной частицы химического элемента.

Что нам скажет Википедия?
Понятие об атоме как о наименьшей неделимой части материи было впервые сформулировано древнеиндийскими и древнегреческими философами (см.: атомизм). В XVII и XVIII веках химикам удалось экспериментально подтвердить эту идею, показав, что некоторые вещества не могут быть подвергнуты дальнейшему расщеплению на составляющие элементы с помощью химических методов. Однако в конце XIX — начале XX века физиками были открыты субатомные частицы и составная структура атома, и стало ясно, что реальная частица, которой было присвоено имя атома, в действительности не является неделимой.
На международном съезде химиков в Карлсруэ (Германия) в 1860 году были приняты определения понятий молекулы и атома. Атом — наименьшая частица химического элемента, входящая в состав простых и сложных веществ.
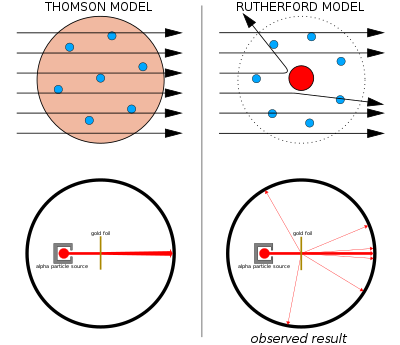
Современная модель атома является развитием планетарной модели Бора-Резерфорда. Согласно современной модели, ядро атома состоит из положительно заряженных протонов и не имеющих заряда нейтронов и окружено отрицательно заряженными электронами. Однако представления квантовой механики не позволяют считать, что электроны движутся вокруг ядра по сколько-нибудь определенным траекториям (неопределенность координаты электрона в атоме может быть сравнима с размерами самого атома).
При описании электронов в атоме в рамках квантовой механики обычно рассматривают распределение вероятности в 3n-мерном пространстве для системы n электронов.
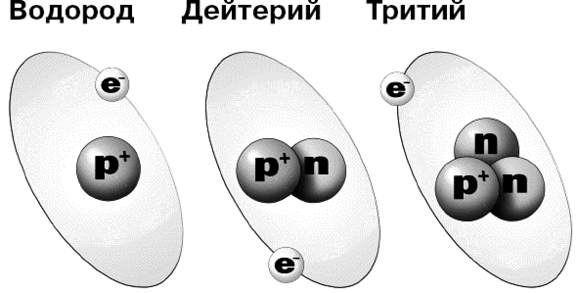
По определению, любые два атома с одним и тем же числом протонов в их ядрах относятся к одному химическому элементу. Атомы с одним и тем же количеством протонов, но разным количеством нейтронов называют изотопами данного элемента. Например, атомы водорода всегда содержат один протон, но существуют изотопы без нейтронов (водород-1, иногда также называемый протием — наиболее распространенная форма), с одним нейтроном (дейтерий) и двумя нейтронами (тритий).
Поскольку наибольший вклад в массу атома вносят протоны и нейтроны, суммарное число этих частиц называют массовым числом. Массу покоя атома часто выражают в атомных единицах массы (а. е. м.), которая также называется дальтоном (Да). Эта единица определяется как 1⁄12 часть массы покоя нейтрального атома углерода-12, которая приблизительно равна 1,66⋅10−24 г. Водород-1 — наилегчайший изотоп водорода и атом с наименьшей массой, имеет атомный вес около 1,007825 а. е. м. Масса атома приблизительно равна произведению массового числа на атомную единицу массы.
Атомы не имеют отчетливо выраженной внешней границы, поэтому их размеры определяются по расстоянию между ядрами одинаковых атомов, которые образовали химическую связь (ковалентный радиус) или по расстоянию до самой дальней из стабильных орбит электронов в электронной оболочке этого атома (радиус атома). Радиус зависит от положения атома в периодической системе, вида химической связи, числа ближайших атомов (координационного числа) и квантово-механического свойства, известного как спин.