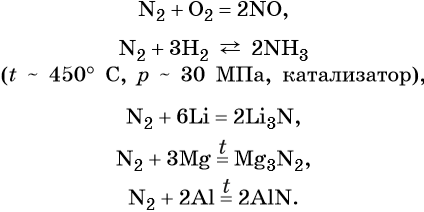Азот - химический элемент, представленный двухатомным газом без цвета, вкуса и запаха. Он является одним из самых распространенных элементов на Земле и составляет большую часть воздуха. В этой статье вы узнаете о свойствах азота, его истории открытия, электронной конфигурации, реакциях и применении в промышленности и научных исследованиях.
Cодержание
Основные свойства азота
Азот (N) — химический элемент, обладающий атомным номером 7. В природе азот представлен двухатомным газом без цвета, вкуса и запаха, обозначаемым химической формулой N2. Он является одним из самых распространенных элементов на Земле и составляет около 78% объема воздуха.
Химически азот является инертным элементом, однако он может реагировать с комплексными соединениями переходных металлов. Азот широко применяется как инертная среда в различных технологических процессах, а жидкий азот используется в качестве хладагента.
Азот также является одним из основных биогенных элементов, который входит в состав белков и нуклеиновых кислот.

История открытия азота
Азот был впервые выделен и описан в 1772 году Генри Кавендишем. Он провел опыты, пропуская воздух над раскаленным углем и затем обрабатывая его щелочью. В результате получался остаток, который Кавендиш назвал удушливым воздухом. Этот остаток, как позднее выяснилось, представлял собой по большей части азот. Однако, Кавендиш не смог понять, что это новое простое вещество, и описал его как мефитический воздух.
В том же году Кавендиш поделился своими результатами с Джозефом Пристли, который также проводил эксперименты связанные с азотом. Однако, из-за преобладающей в то время теории флогистона, Пристли неправильно истолковал свои результаты и считал, что полученный им воздух является флогистированным воздухом.
Существенный вклад в изучение азота внес Даниэль Резерфорд, который в 1772 году опубликовал диссертацию, в которой описал азот как вредный, ядовитый воздух и предположил, что это новый химический элемент.

Электронное строение азота
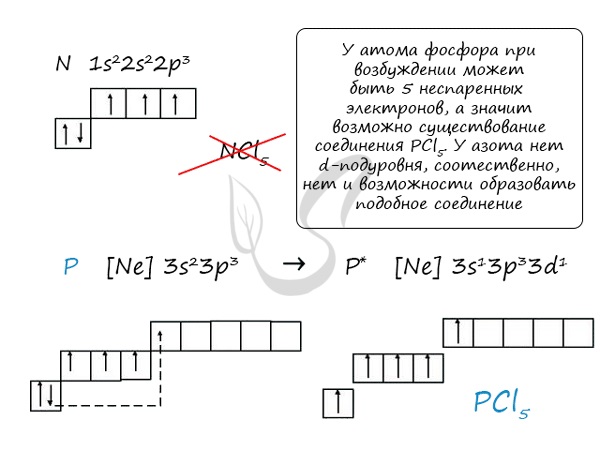
Атом азота имеет атомный номер 7 и электронную конфигурацию 1s2 2s2 2p3. На внешнем энергетическом уровне у азота находятся 5 валентных электронов, что означает, что до завершения его энергетической оболочки не хватает 3 электронов. Таким образом, азот проявляет степень окисления -3 при взаимодействии с металлами и водородом, а положительные степени окисления от +1 до +5 при взаимодействии с кислородом и фтором.
См. также
Реакции азота
Азот реагирует с различными элементами и соединениями при высоких температурах и/или в присутствии катализаторов.
- С металлами азот может образовывать нитриды. Например, при взаимодействии с литием образуется нитрид лития: 6Li + N2 → 2Li3N.
- С водородом азот реагирует при высоком давлении, повышенной температуре и в присутствии катализатора, образуя аммиак: N2 + 3H2 ⇌ 2NH3.
- Азот также проявляет окислительные свойства в реакциях с металлами и водородом. Например, с кальцием образуется нитрид кальция: 3Ca + N2 → Ca3N2.
- Взаимодействие азота с кислородом возможно только при очень высокой температуре и протекает в атмосфере во время грозы. В результате образуется оксид азота: N2 + O2 → 2NO.
Применение азота
Азот широко используется в промышленности и научных исследованиях. Он применяется для получения аммиака и азотных удобрений. Также азот используется для создания инертной среды во время проведения химических реакций. Жидкий азот находит применение в медицине, а также используется для охлаждения в химических и физических исследованиях.

Заключение
Азот является важным химическим элементом, который обладает уникальными свойствами и широким спектром применения. Его реакции с другими элементами и соединениями при высоких температурах позволяют использовать азот в различных технологических процессах.