Азот (N) является одним из самых распространенных и биологически значимых элементов. Узнайте способы получения азота и его свойства.
Cодержание
Введение
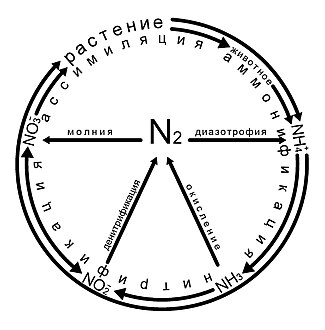
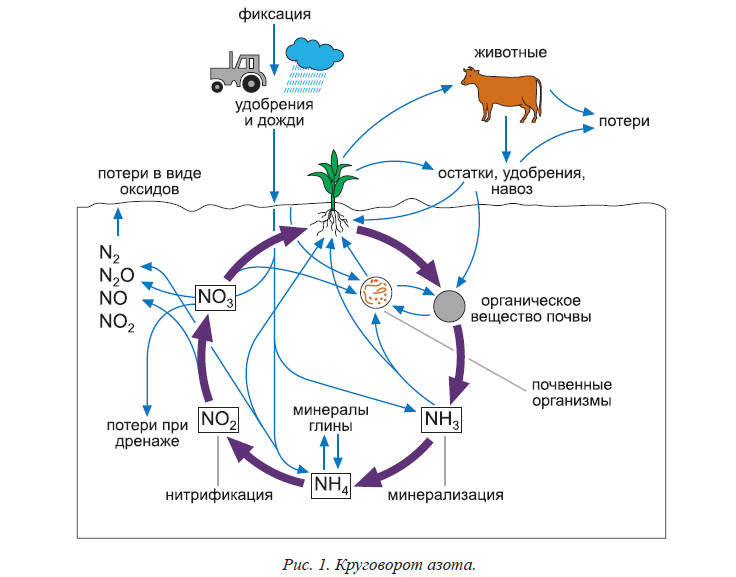
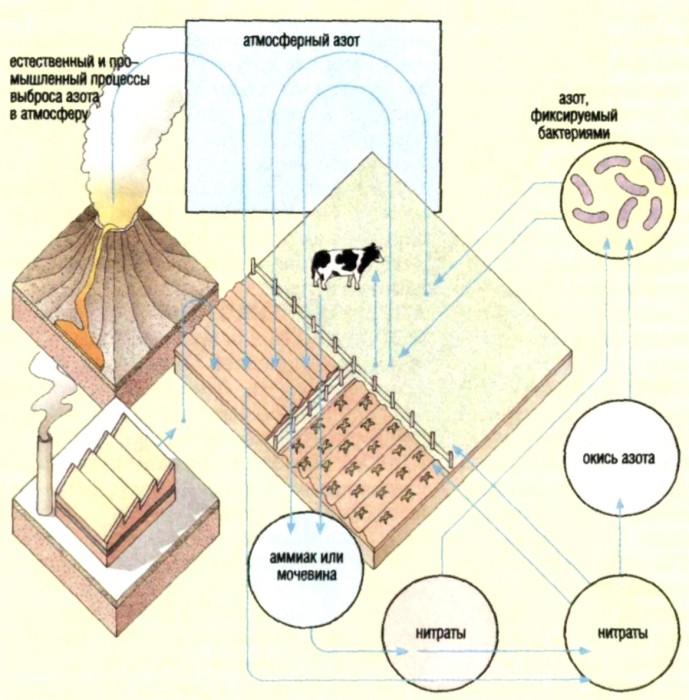
Азот (N) является двухатомным газом, который не имеет вкуса, цвета и запаха. Он является основным компонентом воздуха и одним из самых распространенных и биологически значимых элементов. Азот входит в состав нуклеиновых кислот, гемоглобина, белков и хлорофилла.

Свойства азота
Азот обладает уникальными химическими и физическими свойствами. Он представляет собой двухатомные молекулы N2 и может проявлять свойства окислителя и восстановителя, реагируя как с металлами, так и с неметаллами. Азот вступает в реакцию с кислородом только при высоких температурах и образует аммиак при взаимодействии с водородом. У азота минимальная реакционная способность, для взаимодействия требуются жесткие условия и активные вещества.
Физически азот не растворяется хорошо в воде и не обладает ни цветом, ни запахом. Его плотность составляет 1,2506 кг/м3. Азот может быть твердым при очень низких температурах, образуя белые кристаллы или массу, похожую на снег. В жидком состоянии азот подвижный и не имеет цвета. При взаимодействии с воздухом он вытягивает кислород. В этом состоянии его плотность составляет 808 кг/м3.

Способы получения азота
Существует несколько распространенных способов получения азота.
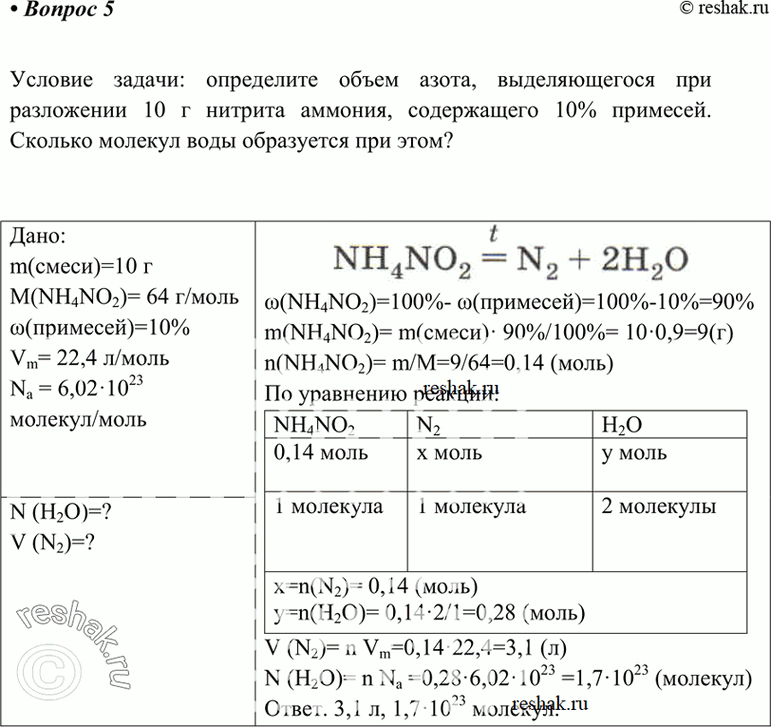
1. Разложение нитрита аммония
В лабораторных условиях азот можно получить путем реакции разложения нитрита аммония (NH4NO2). Для этого в насыщенный подогретый раствор сульфата аммония добавляют насыщенный раствор нитрита натрия. В результате образуется и мгновенно разлагается NH4NO2, освобождая азот.
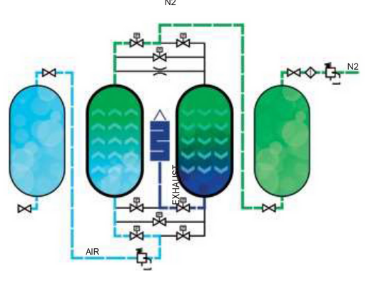
2. Получение азота из атмосферного воздуха
Азот можно получить из атмосферного воздуха путем глубокого охлаждения. Газообразный азот используется для создания инертной атмосферы, хранения и транспортировки легко окисляемых продуктов, процессов обработки металлов и консервации металлических сосудов. Жидкий азот используется как хладагент.
3. Химические способы получения азота
Азот можно получить также с помощью химических реакций. Некоторые из них включают:
- Реакция монооксида азота с озоном;
- Разложение азида натрия;
- Высокотемпературное разложение аммиачной селитры;
- Реакция хлорида аммония и нитрита натрия.
Все эти химические методы получения азота имеют свое практическое применение и используются в различных сферах.
См. также
Заключение
Азот является одним из самых распространенных и биологически значимых элементов. Его получение возможно через различные способы, включая химические реакции и физическое охлаждение. Азот широко используется в различных отраслях, включая производство, металлургию и аналитическую химию.
Что нам скажет Википедия?
Как простое вещество (при н. у.) азот — двухатомный газ (химическая формула — N2) без цвета, вкуса и запаха.
Химически весьма инертен, однако реагирует с комплексными соединениями переходных металлов. Применяется как инертная среда для множества технологических процессов; жидкий азот — хладагент.
История открытия
В 1772 году Генри Кавендиш провёл опыт: он многократно пропускал воздух над раскалённым углём, затем обрабатывал его щёлочью, в результате получался остаток, который Кавендиш назвал удушливым (или мефитическим) воздухом. С позиций современной химии ясно, что в реакции с раскалённым углём кислород воздуха связывался в углекислый газ, который затем поглощался щёлочью. При этом остаток газа представлял собой по большей части азот. Таким образом, Кавендиш выделил азот, но не сумел понять, что это новое простое вещество (химический элемент), и описал его как мефитический воздух (от англ. mephitic — «вредный»). В том же году Кавендиш сообщил об этом опыте Джозефу Пристли.