Уголь (ископаемый уголь) - полезное ископаемое, ценнейший вид топлива и сырье для химической, и не только, промышленности. Узнайте, как образуется уголь, его использование, виды, проблемы выбросов CO2 и аллотропные модификации углерода. Читайте статью на NOCFN.
Cодержание
Уголь (ископаемый уголь) - осадочная порода, полезное ископаемое, ценнейший вид топлива и сырье для химической, и не только, промышленности. Международное название углерода происходит от лат. carbō - "уголь".
Образование угля
Уголь образуется из спор, частей эпидермия плаунов, папоротников и других древних растений, которые существовали 350-250 млн лет назад. Ископаемый уголь классифицируется на различные подвиды, такие как тощие угли, антрациты, коксующиеся, слабоспекающиеся, газовые, длиннопламенные и др. Затем происходит карбонизация, при которой растительный материал преобразуется в уголь под воздействием повышенных температур и без доступа кислорода.
Уголь, после древесины, был первым из используемых человеком видов ископаемого топлива. Сжигание угля позволяет получить значительное количество энергии. В 1960 году уголь давал около половины мирового производства энергии, к 1970 году его доля упала до одной трети.

Использование угля
Уголь широко используется в различных отраслях промышленности. Он является сырьем для производства кокса, используется как материал для рисования, а также из него получают анилиновые красители.
См. также
Виды угля
В зависимости от степени преобразования и удельного количества углерода в угле различаются следующие типы:
- Лигнит: содержит наименьшее количество углерода и обладает низкой теплотворной способностью.
- Бурый уголь: содержит больше углерода, чем лигнит, но все еще имеет низкую теплотворную способность.
- Каменный уголь: более высокое содержание углерода, обеспечивает более высокую теплотворную способность.
- Антрацит: содержит наибольшее количество углерода, обладает высокой теплотворной способностью.

Чистый уголь и проблема выбросов
Сжигание угля приводит к выделению значительного количества CO2, что является проблемой из-за его негативного влияния на климат. Концепция чистого угля предполагает сбор и утилизацию CO2, который образуется при сжигании угля. Одним из способов снижения выбросов является использование чистого кислорода для сжигания угля, что позволяет сократить количество образующегося CO2.
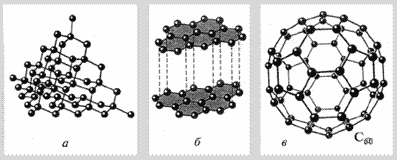
Аллотропные модификации углерода
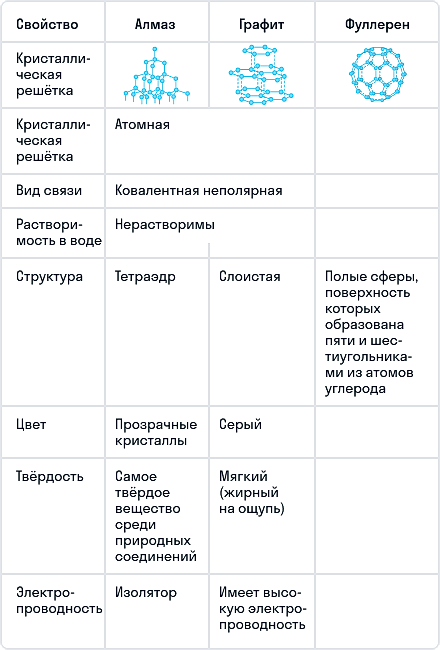
Углерод существует во множестве аллотропных модификаций, которые отличаются своими физическими свойствами и применением:
- Алмаз: самый твердый природный минерал, используется в промышленности для обработки различных материалов.
- Графит: обладает слоистой структурой, используется в качестве смазок, в производстве карандашей и электродов.
Это лишь некоторые из аллотропных модификаций углерода, которые имеют важное значение в различных отраслях науки и промышленности.
См. также
Заключение
Уголь играет важную роль в химической и промышленной отраслях, являясь ценным видом топлива и сырья. Его образование происходит из древних растений под землей без доступа кислорода. Различные типы угля имеют разную степень преобразования и удельное содержание углерода. Проблема выбросов CO2 при сжигании угля ставит перед научным сообществом задачу разработки чистых технологий с утилизацией CO2. Аллотропные модификации углерода, такие как алмаз и графит, имеют широкое применение в различных отраслях промышленности.
Что нам скажет Википедия?
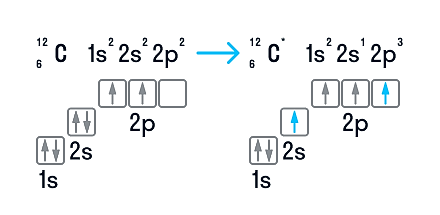
Углерод (химический символ - C, от лат. Carboneum) - химический элемент четырнадцатой группы второго периода (по устаревшей классификации - главной подгруппы четвёртой группы, IVA) периодической системы химических элементов Д. И. Менделеева, с атомным номером 6.
Три изотопа данного элемента встречаются в окружающем нас мире. Изотопы 12C и 13C являются стабильными, в то время как 14C радиоактивный (период полураспада данного изотопа составляет 5730 лет). Углерод был известен ещё в античном мире.
Способность углерода образовывать полимерные цепочки порождает огромный класс соединений на основе углерода, называемых органическими, которых значительно больше, чем неорганических, и изучением которых занимается органическая химия.
В 1791 году английский химик Теннант первым получил свободный углерод; он пропускал пары фосфора над прокалённым мелом, в результате чего образовывались фосфат кальция и углерод. То, что алмаз при сильном нагревании сгорает без остатка, было известно давно. Лавуазье поставил новый опыт по сжиганию алмаза с помощью большой зажигательной машины и пришёл к выводу, что алмаз представляет собой кристаллический углерод.
Основные и хорошо изученные аллотропные модификации углерода - алмаз и графит. При нормальных условиях термодинамически устойчив только графит, а алмаз и другие формы метастабильны. Прямой переход графита в алмаз происходит при 3000 K и давлении 11—12 ГПа. Жидкий углерод существует только при определённом внешнем давлении.
Кристаллическая модификация углерода гексагональной сингонии с цепочечным строением молекул называется карбин. Цепи имеют либо полиеновое строение (−C≡C−), либо поликумуленовое (=C=C=).




![Уголь плюс вода" [1984 Шпулькин Г.Б. - Эта увлекательная химия]](http://chemlib.ru/books/item/f00/s00/z0000038/pic/000113.jpg)



