В этой статье вы узнаете о истории открытия хлора, его распространении в природе, химических свойствах и формулах. Углубитесь в мир элемента CL и его роль в науке. Читайте подробнее на NOCFN.
Cодержание
История открытия хлора
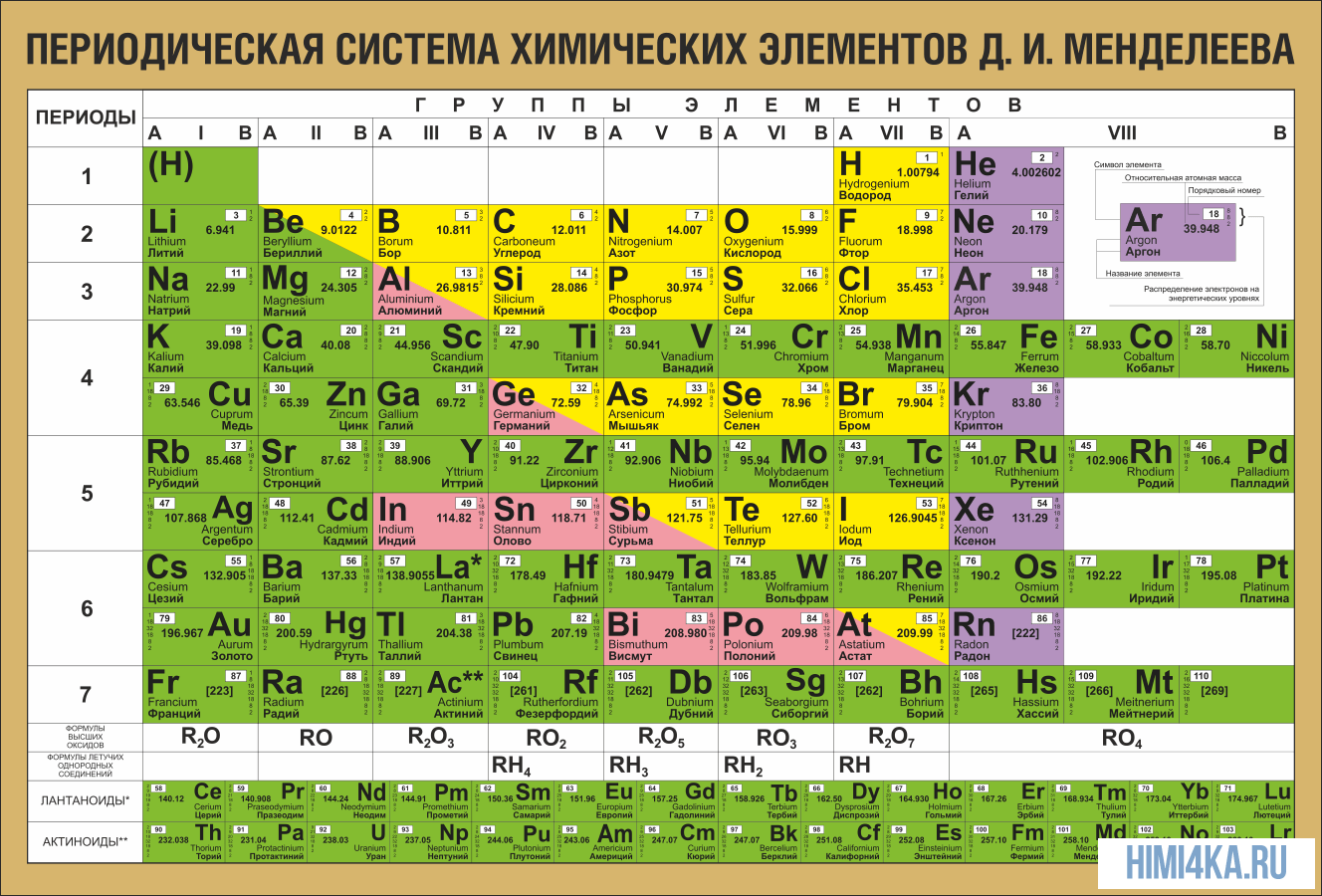
Хлор (химический символ - Cl, от др.-греч. χλωρός - «изжелта-зелёный», от лат. Chlorum) - химический элемент 17-й группы (по устаревшей классификации - главной подгруппы седьмой группы, VIIA) третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 17.
Простое вещество хлор (при нормальных условиях) - ядовитый удушающий двухатомный газ (формула - Cl2) желтовато-зелёного цвета, тяжелее воздуха, с резким запахом и сладковатым, «металлическим» вкусом.
Соединение с водородом - газообразный хлороводород - был впервые получен Джозефом Пристли в 1772 г. Хлор был получен в 1774 г. шведским химиком Карлом Вильгельмом Шееле, описавшим его выделение при взаимодействии пиролюзита с соляной кислотой в своём трактате о пиролюзите.
Шееле отметил запах хлора, схожий с запахом царской водки, его способность взаимодействовать с золотом и киноварью, а также его отбеливающие свойства. Однако Шееле, в соответствии с господствовавшей в химии того времени теорией флогистона, предположил, что хлор представляет собой дефлогистированную муриевую (соляную) кислоту. Бертолле и Лавуазье в рамках кислородной теории кислот обосновали, что новое вещество должно быть оксидом гипотетического элемента мурия. Однако попытки его выделения оставались безуспешными вплоть до работ Г. Дэви, которому электролизом удалось разложить поваренную соль на натрий и хлор, доказав элементарную природу последнего.
В 1811 г. Дэви предложил для нового элемента название «хлорин» (chlorine). Спустя год Ж. Гей-Люссак «сократил» французское название до хлора (chlore), хотя в английском языке оно осталось прежним. В том же 1811 г. немецкий физик Иоганн Швейгер предложил для хлора название «галоген» (дословно солерод), однако впоследствии этот термин закрепился за всей 17-й (VIIA) группой элементов, в которую входит и хлор.
Распространение в природе
В земной коре хлор - самый распространённый галоген. Хлор очень активен - он непосредственно соединяется почти со всеми элементами периодической системы. Поэтому в природе он встречается только в виде соединений в составе минералов: галита NaCl, сильвина KCl, сильвинита KCl·NaCl, бишофита MgCl2·6H2O, карналлита KCl·MgCl2·6H2O, каинита KCl·MgSO4·3H2O. Самые большие запасы хлора содежатся в морской воде.

Химические свойства
Хлор (лат. Сhlorum), Cl (читается «хлор»), химический элемент с атомным номером 17, атомная масса 35, 453. В свободном виде - желто-зеленый тяжелый газ с резким удушливым запахом (отсюда название: греч. chloros - желто-зеленый).
Радиус нейтрального атома хлора 0,099 нм, ионные радиусы равны, соответственно (в скобках указаны значения координационного числа): Cl- 0,167 нм (6), Cl5+ 0,026 нм (3) и Cl7+ 0,022 нм (3) и 0,041 нм (6). Энергии последовательной ионизации нейтрального атома хлора равны, соответственно, 12,97, 23,80, 35,9, 53,5, 67,8, 96,7 и 114,3 эВ. Сродство к электрону 3,614 эВ. По шкале Полинга электроотрицательность хлора 3,16.
Важнейшее химическое соединение хлора - поваренная соль (химическая формула NaCl, химическое название хлорид натрия) - было известно человеку с древнейших времен. Имеются свидетельства того, что добыча поваренной соли осуществлялась еще 3-4 тысячи лет до нашей эры в Ливии. Возможно, что, используя поваренную соль для различных манипуляций, алхимики сталкивались и с газообразным хлором. Для растворения «царя металлов» - золота - они использовали «царскую водку» - смесь соляной и азотной кислот, при взаимодействии которых выделяется хлор.
Впервые газ хлор получил и подробно описал шведский химик К. Шееле в 1774 году. Он нагревал соляную кислоту с минералом пиролюзитом и наблюдал выделение желто-зеленого газа с резким запахом. Так как в те времена господствовала теория флогистона, новый газ Шееле рассматривал как «дефлогистонированную соляную кислоту», т.е. как оксид (окись) соляной кислоты. А. Лавуазье рассматривал газ как оксид элемента «мурия» (соляную кислоту называли муриевой, от лат. muria - рассол). Такую же точку зрения сначала разделял английский ученый Г. Дэви, который потратил много времени на то, чтобы разложить «окись мурия» на простые вещества. Это ему не удалось, и к 1811 году Дэви пришел к выводу, что данный газ - это простое вещество, и ему отвечает химический элемент. Дэви первым предложил в соответствие с желто-зеленой окраской газа назвать его chlorine (хлорин). Название «хлор» элементу дал в 1812 французский химик Ж. Л. Гей-Люссак; оно принято во всех странах, кроме Великобритании и США, где сохранилось название, введенное Дэви. Высказывалось мнение о том, что данный элемент следует назвать «галоген» (т.е. рождающий соли), но оно со временем стало общим названием всех элементов группы VIIA.
См. также
Химические формулы и знаки
Химический знак или химический символ элемента - это первая или две первые буквы от латинского названия этого элемента. Название химического знака в большинстве случаев читается как название химического элемента. Например, К - калий, Са - кальций, Mg - магний, Mn - марганец.
| Химический знак | Чтение |
|---|---|
| К | калий |
| Са | кальций |
| Mg | магний |
| Mn | марганец |
Химические формулы простых веществ (всех металлов и многих неметаллов) являются знаки соответствующих химических элементов. Например, вещество железо и химический элемент железо обозначаются одинаково - Fe.
| Химический знак | Чтение |
|---|---|
| Fe | железо |
| Na | натрий |
| O2 | кислород |
| N2 | азот |
Формулу сложного вещества составляют путем записи знаков химических элементов, из которых это вещество состоит, с указанием числа атомов каждого элемента в молекуле.
| Химический знак | Чтение |
|---|---|
| H2O | вода |
| CaSO4 | гипс |
| Al2O3 | алюминий оксид |
| CS2 | уголь дисульфид |
Исключение составляют вещества, существующие в виде димеров, которые записываются с индексом внизу справа от знака каждого элемента. Например, N2O4, P4O6, P4O10.
Заключение
Хлор (Cl) - химический элемент 17-й группы периодической системы, который был впервые получен Карлом Вильгельмом Шееле в 1774 году. Он является самым распространенным галогеном в природе и образует соединения с практически всеми элементами. Название химического знака Cl происходит от древнегреческого слова χλωρός, что означает «изжелта-зеленая». Чтение химических знаков и формул зависит от названия химического элемента и структуры вещества. Изучение свойств и химической формулы хлора позволяет лучше понимать его роль и применение в различных процессах и отраслях науки.
Что нам скажет Википедия?
Как читается элемент CL? Название химического элемента Cl, соответствующее символу, происходит от древнегреческого слова χλωρός, что означает «изжелта-зеленая». Впервые хлор был получен шведским химиком Карлом Вильгельмом Шееле в 1774 году. Он описал процесс получения хлора при взаимодействии пиролюзита с соляной кислотой и отметил его запах, похожий на запах царской водки, а также его отбеливающие свойства. В то время хлор был предположительно считался дефлогистированной муриевой (соляной) кислотой, соответствуя теории флогистона. Однако позднее исследования Г. Дэви показали, что хлор является самостоятельным элементом.
В 1811 году Дэви предложил название «хлорин» для нового элемента, а Ж. Гей-Люссак сократил французское название до «хлор». Хлор является самым распространенным галогеном в земной коре и образует соединения с практически всеми элементами периодической системы. Он встречается в природе в виде соединений в минералах, таких как галита, сильвина и карналлит, а также в морской воде.
Атом хлора имеет два стабильных изотопа с массовыми числами 35 и 37. Хлор является сильным окислителем и может образовывать оксиды с разными степенями окисления. Он также реагирует с металлами и неметаллами, образуя соответствующие хлориды. Хлор имеет множество применений, включая использование в процессах отбеливания, производстве хлорированных органических соединений и водоочистке.