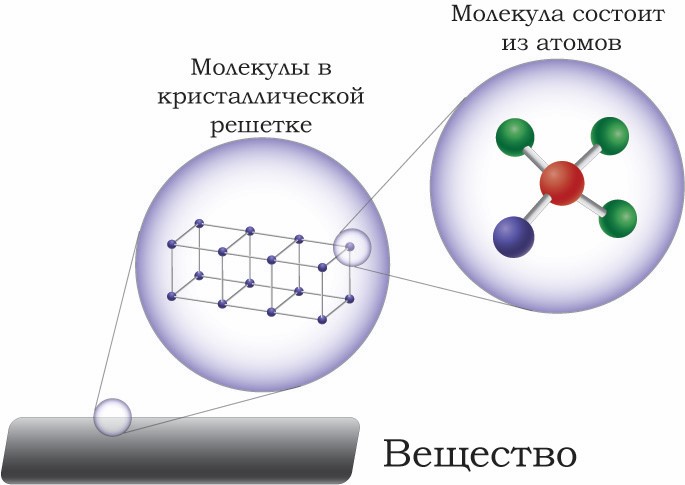
В 1913 году Нильс Бор предложил теорию строения атомов, основанную на планетарной модели. Атомы состоят из электронов, протонов и нейтронов. Узнайте больше о составе атома и его важной роли в химических и физических процессах в мире.
Cодержание
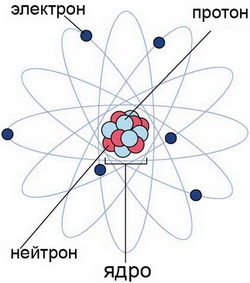
В 1913 году датский физик Нильс Бор предложил свою теорию строения атома, основанную на планетарной модели, предложенной физиком Резерфордом. В этой модели атом уподобляется планетарной системе, где электроны движутся по орбитам вокруг ядра атома, подобно планетам, движущимся вокруг звезды.
Бор внёс в свою теорию идею квантования, согласно которой электроны могут двигаться только по фиксированным орбитам, соответствующим определённым энергетическим уровням. Это привело к созданию современной квантово-механической модели атома, в которой ядро атома, состоящее из протонов и нейтронов, окружено электронами.
Состав атома
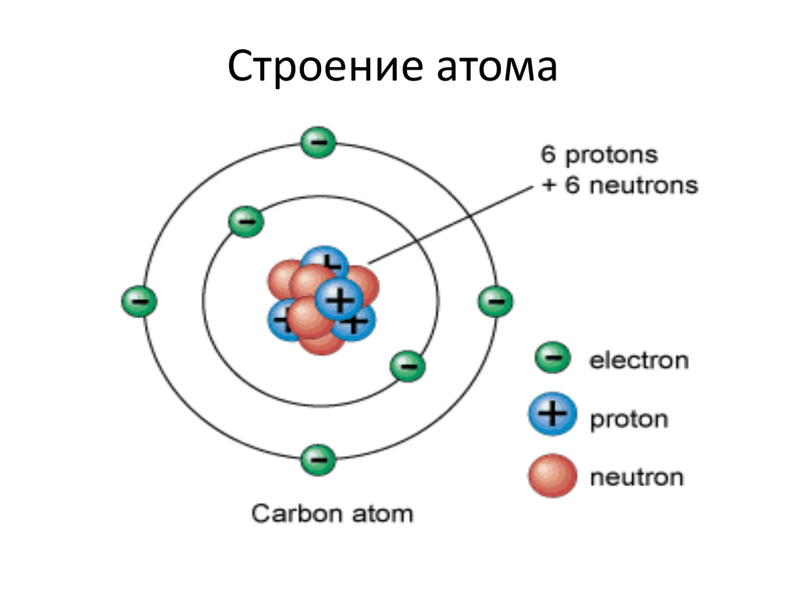
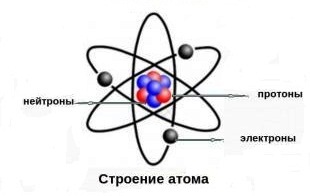
Атомы состоят из трёх основных частиц: электронов, протонов и нейтронов. Нейтроны были открыты в 1932 году, после разработки планетарной модели атома. Нейтроны не имеют заряда и не реагируют на электромагнитное поле.
Ядро атома состоит из протонов и нейтронов. Протоны являются тяжелыми частицами с положительным зарядом, а нейтроны не имеют заряда. Обе эти частицы имеют схожие размеры, но протоны почти в две тысячи раз тяжелее электронов.
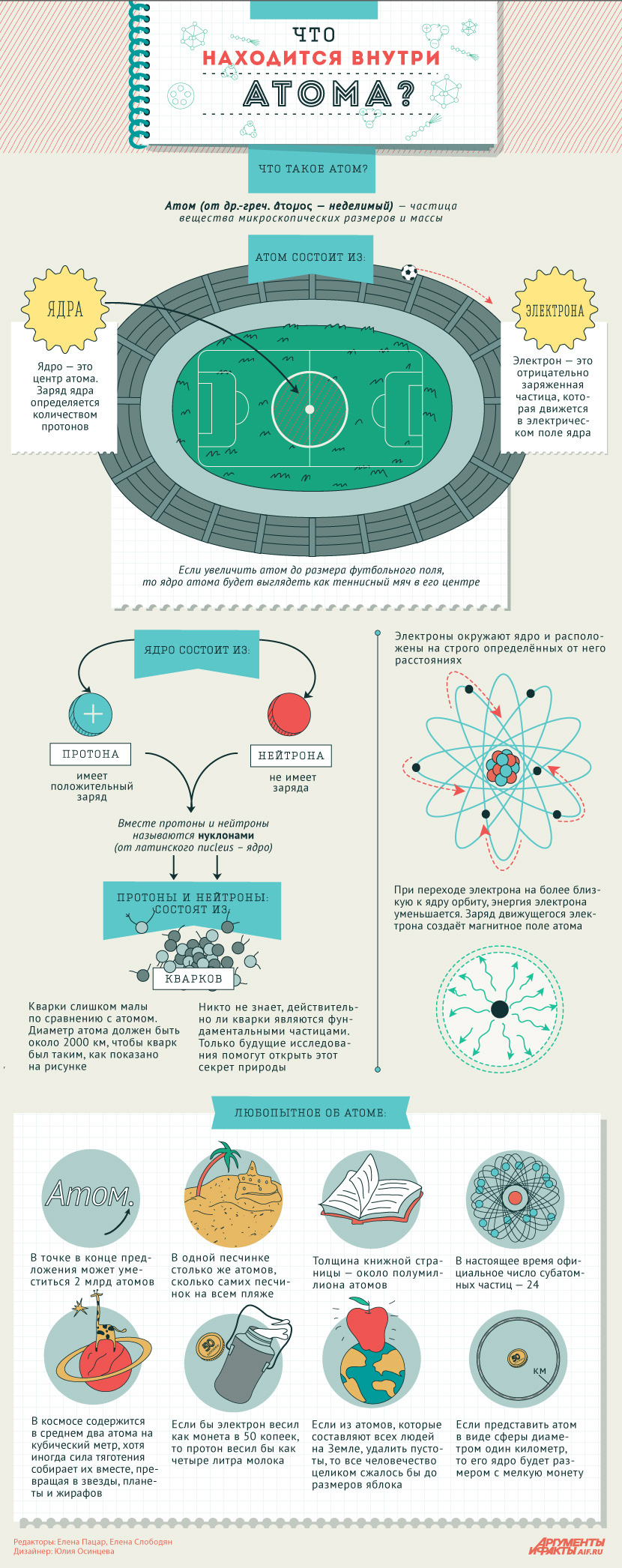
В свою очередь, протоны и нейтроны состоят из элементарных частиц, называемых кварками. Кварки являются самой маленькой основной частицей материи в современной физике.
Структура атома
Атомы имеют общую структуру, включающую атомное ядро и электронную оболочку. Оболочка состоит из электронов и определяет свойства вещества в зависимости от их количества.
Атомное ядро, несущее большую часть массы атома, состоит из протонов и нейтронов. Количество протонов определяет порядковый номер атома в периодической системе Менделеева и его принадлежность к определённому химическому элементу. Если число протонов равно числу электронов, атом является электрически нейтральным. В противном случае атом обладает зарядом и называется ионом.
Важно отметить, что размеры атомного ядра крайне малы по сравнению с размерами атома в целом. Если увеличить атом до размеров футбольного поля, то размеры его ядра будут сравнимы с теннисным мячом в центре поля.
См. также
Разнообразие атомов
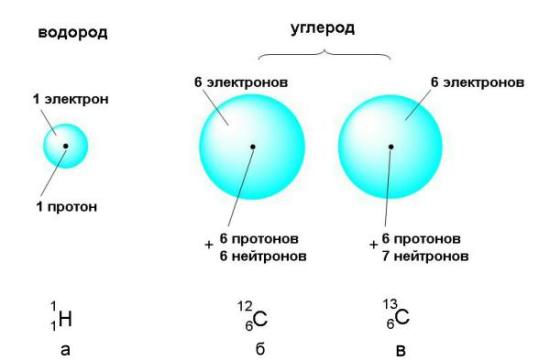
В природе существует множество различных атомов, которые отличаются размерами, массой и другими характеристиками. Совокупность атомов одного вида называется химическим элементом. На данный момент известно более ста химических элементов, каждый из которых имеет уникальные свойства.
В заключение, атомы являются основными строительными блоками материи. Они состоят из электронов, протонов и нейтронов. Структура атома включает ядро и электронную оболочку. Разнообразие атомов определяется их составом и свойствами. Изучение строения атома и его взаимодействия имеет фундаментальное значение для понимания химических и физических процессов в мире.

Что нам скажет Википедия?
Атомы состоят из ядра и электронов (точнее, электронного «облака»). Ядро атома состоит из протонов и нейтронов. Количество нейтронов в ядре может быть разным: от нуля до нескольких десятков. Если число электронов совпадает с числом протонов в ядре, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом. В некоторых случаях под атомами понимают только электронейтральные системы, в которых заряд ядра равен суммарному заряду электронов, тем самым противопоставляя их электрически заряженным ионам.
Ядро, несущее почти всю (более чем 99,9 %) массу атома, состоит из положительно заряженных протонов и незаряженных нейтронов, связанных между собой при помощи сильного взаимодействия. Атомы классифицируются по количеству протонов и нейтронов в ядре: число протонов Z соответствует порядковому номеру атома в периодической системе Менделеева и определяет его принадлежность к некоторому химическому элементу, а число нейтронов N — определённому изотопу этого элемента. Единственный стабильный атом, не содержащий нейтронов в ядре — лёгкий водород (протий). Число Z также определяет суммарный положительный электрический заряд (Z×e) атомного ядра и число электронов в нейтральном атоме, задающее его размер.