Узнайте о различиях между S и P орбиталями. Форма, симметрия, расположение и протяженность - все объясняется в этой статье.
Cодержание
Орбитали являются одноэлектронными волновыми функциями, описывающими электронное облако в атоме. Совокупность орбиталей с одним значением главного квантового числа n формируют одну электронную оболочку. Атом каждого элемента имеет полный набор орбиталей, которые заполняются электронами по порядку увеличения порядкового номера элемента.

Форма и симметрия
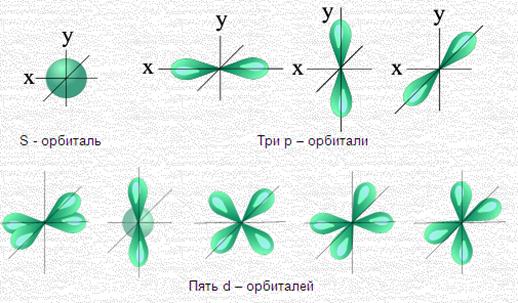
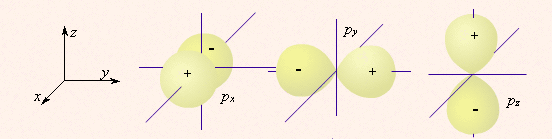
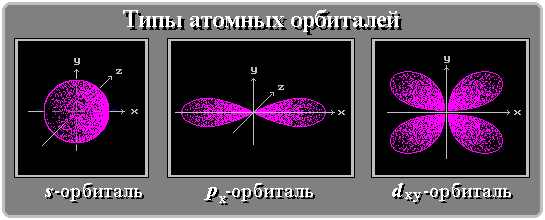
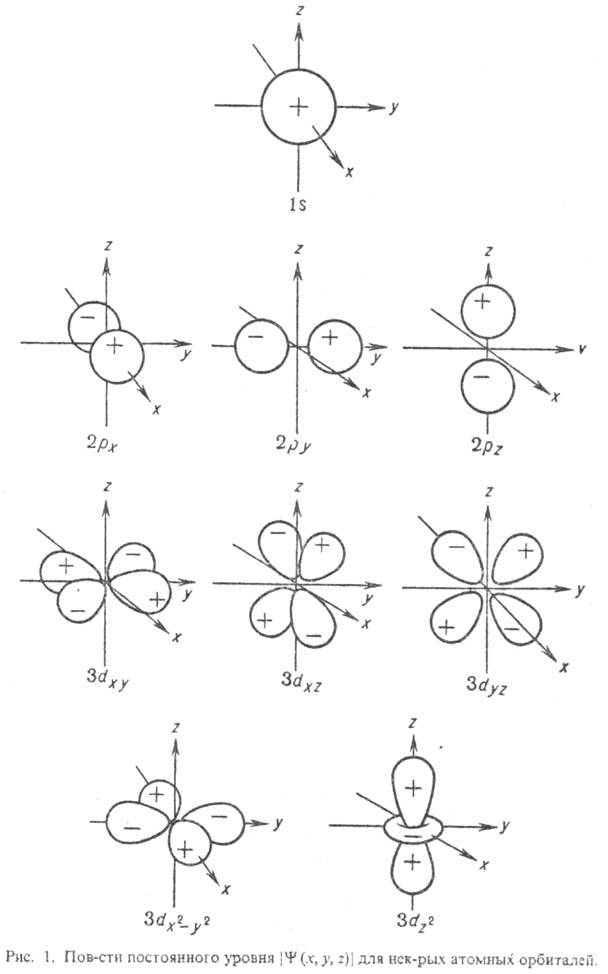
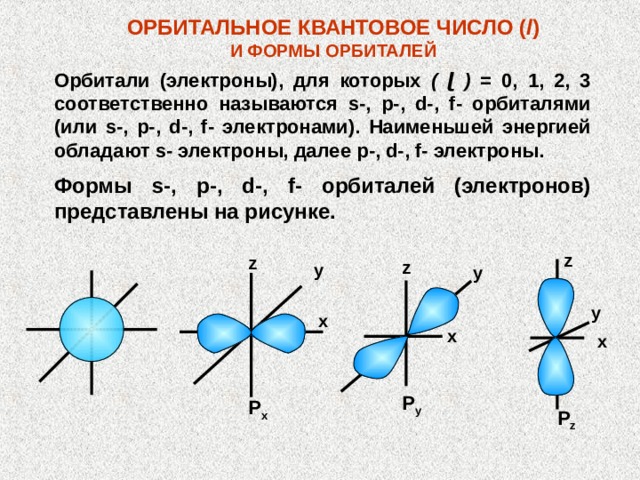
Отличительной особенностью S и P орбиталей является их форма и симметрия. S-орбитали имеют сферическую симметрию, в то время как P-орбитали имеют более сложную конфигурацию, определяемую угловыми частями волновой функции. Угловая зависимость вероятности нахождения электрона в P-орбиталях описывается сферическими функциями Ylm(θ, φ), которые описывают угловую зависимость вероятности нахождения электрона в центральном поле атома.

Расположение и протяженность
Кроме того, S-орбитали являются более близкими к ядру атома и имеют более высокую вероятность нахождения электрона внутри него, в то время как P-орбитали имеют большую протяженность и более высокую вероятность нахождения электрона в окрестности ядра. Визуально S-орбитали представляются в виде сферического электронного облака, а P-орбитали имеют форму двух грушевидных облаков, ориентированных вдоль осей координат.
См. также
Что нам скажет Википедия?
Чем отличаются S и P орбитали?
Орбитали являются одноэлектронными волновыми функциями, описывающими электронное облако в атоме. Совокупность орбиталей с одним значением главного квантового числа n формируют одну электронную оболочку. Атом каждого элемента имеет полный набор орбиталей, которые заполняются электронами по порядку увеличения порядкового номера элемента.
Отличительной особенностью S и P орбиталей является их форма и симметрия. S-орбитали имеют сферическую симметрию, в то время как P-орбитали имеют более сложную конфигурацию, определяемую угловыми частями волновой функции. Угловая зависимость вероятности нахождения электрона в P-орбиталях описывается сферическими функциями Ylm(θ, φ), которые описывают угловую зависимость вероятности нахождения электрона в центральном поле атома.
Кроме того, S-орбитали являются более близкими к ядру атома и имеют более высокую вероятность нахождения электрона внутри него, в то время как P-орбитали имеют большую протяженность и более высокую вероятность нахождения электрона в окрестности ядра. Визуально S-орбитали представляются в виде сферического электронного облака, а P-орбитали имеют форму двух грушевидных облаков, ориентированных вдоль осей координат.