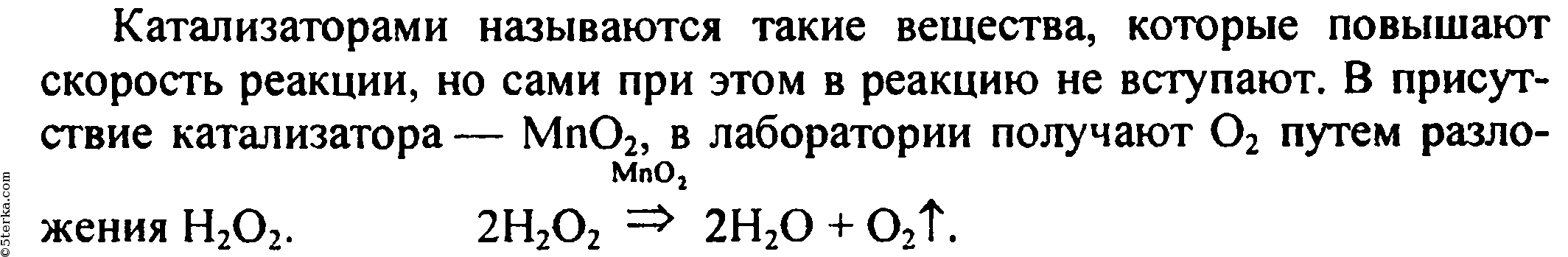Узнайте, какие вещества играют роль катализаторов в химических реакциях. Различные типы катализаторов, их роль и применение в науке и промышленности. От гомогенных до гетерогенных катализаторов. Читайте на NOCFN.
Cодержание
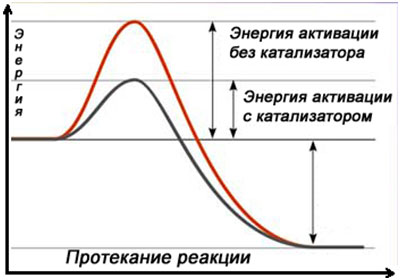
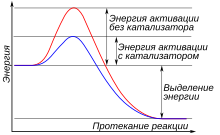
Катализаторы играют важную роль в химических реакциях, ускоряя их протекание без расходования самих катализаторов. Они могут быть разделены на две основные категории - гомогенные и гетерогенные.
Гомогенные катализаторы
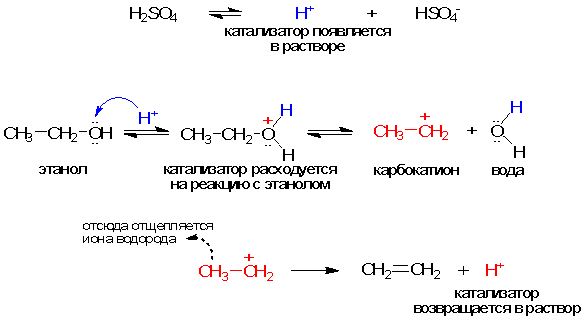
Гомогенные катализаторы находятся в одной фазе с реагирующими веществами. Некоторыми типичными примерами гомогенных катализаторов являются кислоты и основания. Они могут вступать в реакцию с реагентами и образовывать промежуточные соединения, которые ускоряют саму реакцию.

Гетерогенные катализаторы
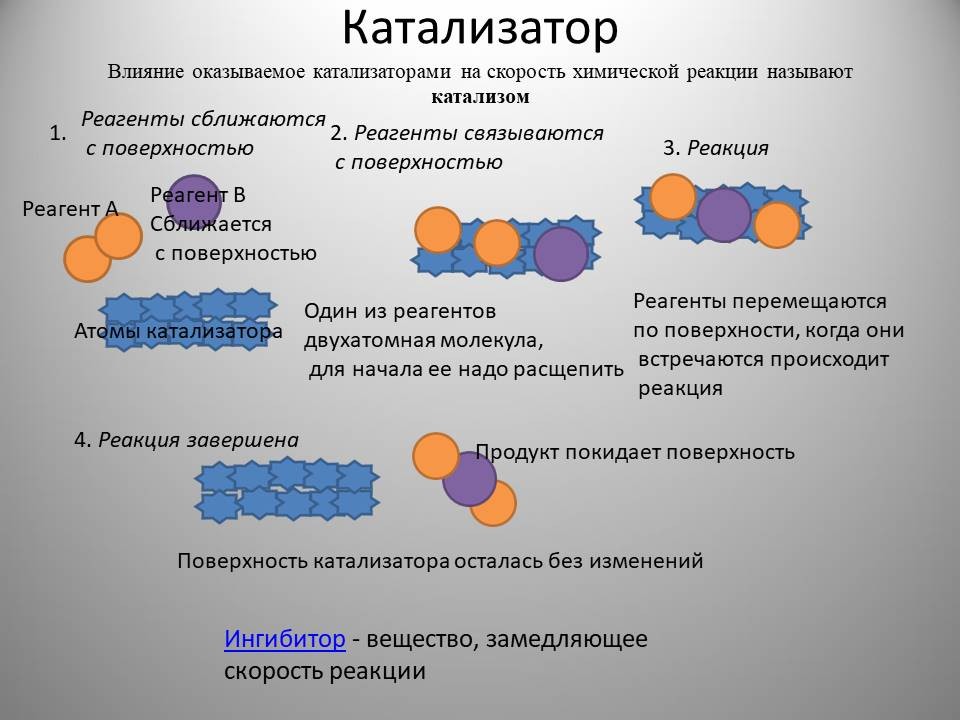
Гетерогенные катализаторы, напротив, образуют отдельную фазу, отделенную от фазы, в которой находятся реагирующие вещества. Типичными гетерогенными катализаторами являются металлы, их оксиды и сульфиды. Они обладают сильно развитой поверхностью и могут быть размещены на инертных носителях, таких как силикагель или оксид алюминия.
См. также
Различные типы катализаторов
Для каждого типа реакции существуют определенные катализаторы, которые эффективно ускоряют протекание реакции. Кислотно-основные катализаторы широко используются, но также существуют катализаторы окисления-восстановления, которые содержат переходные металлы или их соединения. Координационные катализаторы действуют через координацию реагентов у атома или иона переходного металла. Если катализатор обладает хиральными свойствами, то он способен превращать оптически неактивный субстрат в оптически активный продукт.
Роль катализаторов
Катализаторы широко применяются в науке и технике. Они играют важную роль в переработке нефти, производстве различных продуктов и создании новых материалов, таких как пластмассы. Без катализаторов невозможно обеспечить производство моторных топлив, соответствующих экологическим стандартам. Например, в каталитическом крекинге и гидрокрекинге, катализаторы позволяют получать высококачественные нефтепродукты.
Применение катализаторов в биохимических реакциях
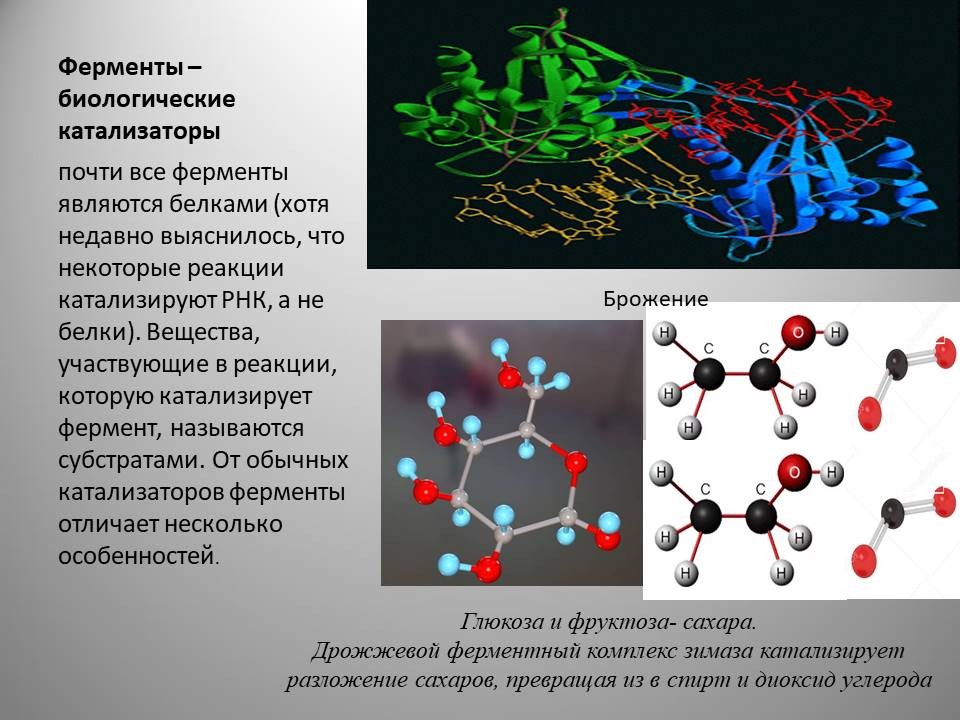
В биохимических реакциях роль катализаторов играют ферменты. Они способны ускорять сложные биохимические процессы, обеспечивая эффективность и специфичность реакций в организмах.
В современной науке и технике часто используются системы из нескольких катализаторов, которые сотрудничают и ускоряют разные стадии реакции. Это позволяет достичь более высокой эффективности и контроля в каталитических процессах.
Катализаторы имеют огромное значение в химических процессах и играют ключевую роль в различных отраслях промышленности. Их постоянное развитие и изучение новых типов катализаторов позволяют улучшать производственные процессы и создавать новые материалы, способствуя прогрессу и инновациям.
См. также
Что нам скажет Википедия?
Катализатор — химическое вещество, ускоряющее реакцию, но не расходующееся в процессе реакции.
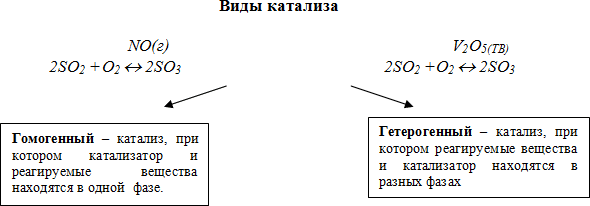
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO.
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня.
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен, так как противоречит закону сохранения энергии: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Основная статья: Каталитический конвертер
Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
- углеводороды (несгоревший бензин, ароматические углеводороды);
- углекислый газ (СО2);
- окиси азота (NOx);
- тяжелые металлы (свинец, ртуть, кадмий).